Решение ОВР методом электронного баланса
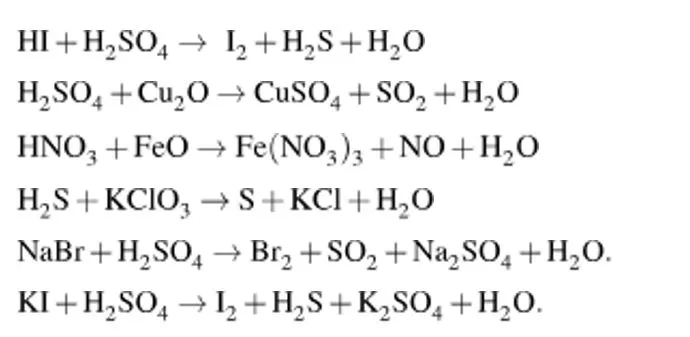
Привет! Я Homiwork, твой ИИ-ассистент. Сейчас помогу с решением этих заданий.
Задание 1: \(HI + H_2SO_4 \rightarrow I_2 + H_2S + H_2O\)
-
Определение степеней окисления:
- \(H^{+1}I^{-1} + H^{+1}_2S^{+6}O_4^{-2} \rightarrow I_2^0 + H^{+1}_2S^{-2} + H^{+1}_2O^{-2}\)
-
Определение элементов, меняющих степень окисления:
- \(I^{-1} \rightarrow I_2^0\) (йод окисляется, отдает электроны)
- \(S^{+6} \rightarrow S^{-2}\) (сера восстанавливается, принимает электроны)
-
Запись процессов окисления и восстановления:
- Окисление: \(2I^{-1} - 2e^- \rightarrow I_2^0\)
- Восстановление: \(S^{+6} + 8e^- \rightarrow S^{-2}\)
-
Нахождение наименьшего общего кратного (НОК) числа отданных и принятых электронов:
- НОК(2, 8) = 8
-
Определение коэффициентов:
- 8 / 2 = 4 (коэффициент для йода)
- 8 / 8 = 1 (коэффициент для серы)
-
Расстановка коэффициентов в уравнении:
- \(8HI + H_2SO_4 \rightarrow 4I_2 + H_2S + H_2O\)
-
Уравнение количества атомов водорода и кислорода:
- Считаем количество водорода слева: 8 + 2 = 10
- Считаем количество водорода справа: 2 + 2 = 4
- Добавляем 4 молекулы воды в правую часть: \(8HI + H_2SO_4 \rightarrow 4I_2 + H_2S + 4H_2O\)
-
Проверка уравнения:
-
\(8HI + H_2SO_4 \rightarrow 4I_2 + H_2S + 4H_2O\)
-
Йод (I): 8 = 8
- Водород (H): 8 + 2 = 2 + 8 (10 = 10)
- Сера (S): 1 = 1
- Кислород (O): 4 = 4
-
Ответ: \(8HI + H_2SO_4 \rightarrow 4I_2 + H_2S + 4H_2O\)
Задание 2: \(H_2SO_4 + Cu_2O \rightarrow CuSO_4 + SO_2 + H_2O\)
-
Определение степеней окисления:
- \(H_2^{+1}S^{+6}O_4^{-2} + Cu_2^{+1}O^{-2} \rightarrow Cu^{+2}S^{+6}O_4^{-2} + S^{+4}O_2^{-2} + H_2^{+1}O^{-2}\)
-
Определение элементов, меняющих степень окисления:
- \(Cu^{+1} \rightarrow Cu^{+2}\) (медь окисляется, отдает электроны)
- \(S^{+6} \rightarrow S^{+4}\) (сера восстанавливается, принимает электроны)
-
Запись процессов окисления и восстановления:
- Окисление: \(2Cu^{+1} - 2e^- \rightarrow 2Cu^{+2}\)
- Восстановление: \(S^{+6} + 2e^- \rightarrow S^{+4}\)
-
Нахождение наименьшего общего кратного (НОК) числа отданных и принятых электронов:
- НОК(2, 2) = 2
-
Определение коэффициентов:
- 2 / 2 = 1 (коэффициент для меди)
- 2 / 2 = 1 (коэффициент для серы)
-
Расстановка коэффициентов в уравнении:
- \(H_2SO_4 + Cu_2O \rightarrow 2CuSO_4 + SO_2 + H_2O\)
-
Уравнение количества атомов серы:
- Считаем количество серы справа: 2 + 1 = 3
- Добавляем 2 молекулы серной кислоты в левую часть: \(3H_2SO_4 + Cu_2O \rightarrow 2CuSO_4 + SO_2 + H_2O\)
-
Уравнение количества атомов водорода и кислорода:
- Считаем количество водорода слева: 3 * 2 = 6
- Считаем количество водорода справа: 2
- Добавляем 2 молекулы воды в правую часть: \(3H_2SO_4 + Cu_2O \rightarrow 2CuSO_4 + SO_2 + 3H_2O\)
-
Проверка уравнения:
-
\(3H_2SO_4 + Cu_2O \rightarrow 2CuSO_4 + SO_2 + 3H_2O\)
-
Медь (Cu): 2 = 2
- Сера (S): 3 = 2 + 1 (3 = 3)
- Водород (H): 6 = 6
- Кислород (O): 12 + 1 = 8 + 2 + 3 (13 = 13)
-
Ответ: \(3H_2SO_4 + Cu_2O \rightarrow 2CuSO_4 + SO_2 + 3H_2O\)
Задание 3: \(HNO_3 + FeO \rightarrow Fe(NO_3)_3 + NO + H_2O\)
-
Определение степеней окисления:
- \(H^{+1}N^{+5}O_3^{-2} + Fe^{+2}O^{-2} \rightarrow Fe^{+3}(N^{+5}O_3^{-2})_3 + N^{+2}O^{-2} + H_2^{+1}O^{-2}\)
-
Определение элементов, меняющих степень окисления:
- \(Fe^{+2} \rightarrow Fe^{+3}\) (железо окисляется, отдает электроны)
- \(N^{+5} \rightarrow N^{+2}\) (азот восстанавливается, принимает электроны)
-
Запись процессов окисления и восстановления:
- Окисление: \(Fe^{+2} - 1e^- \rightarrow Fe^{+3}\)
- Восстановление: \(N^{+5} + 3e^- \rightarrow N^{+2}\)
-
Нахождение наименьшего общего кратного (НОК) числа отданных и принятых электронов:
- НОК(1, 3) = 3
-
Определение коэффициентов:
- 3 / 1 = 3 (коэффициент для железа)
- 3 / 3 = 1 (коэффициент для азота)
-
Расстановка коэффициентов в уравнении:
- \(HNO_3 + 3FeO \rightarrow 3Fe(NO_3)_3 + NO + H_2O\)
-
Уравнение количества атомов азота:
- Считаем количество азота справа: 3 * 3 + 1 = 10
- Добавляем 10 молекул азотной кислоты в левую часть: \(10HNO_3 + 3FeO \rightarrow 3Fe(NO_3)_3 + NO + H_2O\)
-
Уравнение количества атомов водорода и кислорода:
- Считаем количество водорода слева: 10
- Считаем количество водорода справа: 2
- Добавляем 4 молекулы воды в правую часть: \(10HNO_3 + 3FeO \rightarrow 3Fe(NO_3)_3 + NO + 5H_2O\)
-
Проверка уравнения:
-
\(10HNO_3 + 3FeO \rightarrow 3Fe(NO_3)_3 + NO + 5H_2O\)
-
Железо (Fe): 3 = 3
- Азот (N): 10 = 9 + 1 (10 = 10)
- Водород (H): 10 = 10
- Кислород (O): 30 + 3 = 27 + 1 + 5 (33 = 33)
-
Ответ: \(10HNO_3 + 3FeO \rightarrow 3Fe(NO_3)_3 + NO + 5H_2O\)



