Calcolo pH soluzione acquosa H₂SO₄ e MgCl₂
Okay, analizziamo e risolviamo il problema di chimica.
Lingua del compito: Italiano
Задание 1
Testo del problema:
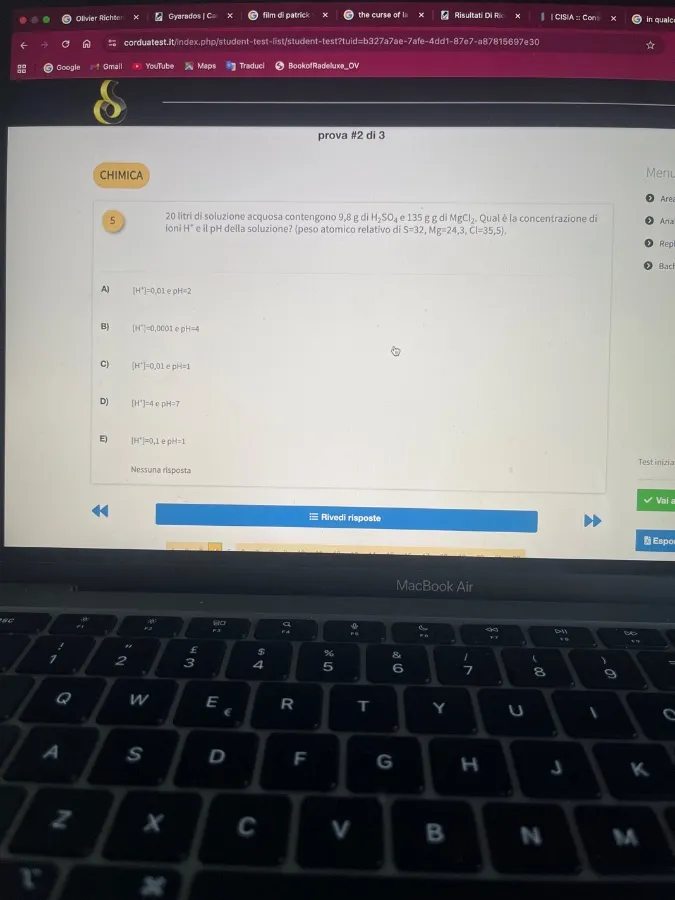
20 litri di soluzione acquosa contengono 9,8 g di H₂SO₄ e 135 g di MgCl₂. Qual è la concentrazione di ioni H⁺ e il pH della soluzione? (peso atomico relativo di S=32, Mg=24,3, Cl=35,5).
Soluzione:
-
Calcolare le moli di H₂SO₄:
- Peso molecolare di H₂SO₄ = 2(1) + 32 + 4(16) = 2 + 32 + 64 = 98 g/mol
- Moli di H₂SO₄ = \(\frac{9.8 \text{ g}}{98 \text{ g/mol}} = 0.1 \text{ mol}\)
-
Calcolare le moli di MgCl₂:
- Peso molecolare di MgCl₂ = 24.3 + 2(35.5) = 24.3 + 71 = 95.3 g/mol
- Moli di MgCl₂ = \(\frac{135 \text{ g}}{95.3 \text{ g/mol}} \approx 1.416 \text{ mol}\)
-
Calcolare la concentrazione di H⁺ derivante da H₂SO₄:
- H₂SO₄ è un acido forte che si dissocia completamente in acqua: H₂SO₄ → 2H⁺ + SO₄²⁻
- Quindi, 0.1 mol di H₂SO₄ produce 2 * 0.1 = 0.2 mol di H⁺
- Concentrazione di H⁺ = \(\frac{0.2 \text{ mol}}{20 \text{ L}} = 0.01 \text{ M}\)
-
MgCl₂ non contribuisce alla concentrazione di H⁺.
-
Calcolare il pH:
- pH = -log[H⁺] = -log(0.01) = -log(10⁻²) = -(-2) = 2
Risposta:
[H⁺] = 0.01 M e pH = 2
Quindi, la risposta corretta è A) [H⁺] = 0,01 e pH = 2
Certo, posso spiegarti come trovare il pH senza usare direttamente la funzione logaritmo sulla calcolatrice.
Il pH è definito come il logaritmo negativo in base 10 della concentrazione degli ioni idrogeno (H⁺):
\(pH = -log_{10}[H^+]\)
Nel nostro caso, abbiamo calcolato che la concentrazione di H⁺ è 0.01 M. Possiamo esprimere 0.01 come una potenza di 10:
\(0.01 = 10^{-2}\)
Quindi, possiamo riscrivere la formula del pH come:
\(pH = -log_{10}(10^{-2})\)
Per la proprietà dei logaritmi, \(log_{b}(b^x) = x\). In questo caso, \(log_{10}(10^{-2}) = -2\).
Quindi,
\(pH = -(-2) = 2\)
In pratica, quando la concentrazione di H⁺ è una potenza di 10 (ad esempio, 0.1, 0.01, 0.001, ecc.), il pH è semplicemente l'esponente cambiato di segno.
- Se \([H^+] = 10^{-1} = 0.1 M\), allora pH = 1
- Se \([H^+] = 10^{-2} = 0.01 M\), allora pH = 2
- Se \([H^+] = 10^{-3} = 0.001 M\), allora pH = 3
E così via. Questo metodo funziona bene quando la concentrazione di H⁺ è una potenza intera di 10.
Risposta:
Il pH della soluzione è 2.
"L elevato a -1" si riferisce a \(L^{-1}\), che è un modo per esprimere l'inverso di litri (L). In termini di unità di misura, \(L^{-1}\) significa "per litro" o "inverso di litro".
Ad esempio, se hai una concentrazione espressa in moli per litro (mol/L), puoi anche scriverla come mol * \(L^{-1}\) (mol * per litro).
Quindi, \(L^{-1}\) è semplicemente un modo matematico per indicare che i litri sono al denominatore di una frazione o che si sta parlando di una quantità "per litro".



